Differenza tra nitrato e nitrite
Sia nitrato che nitrito sono anioni ossia di azoto. Anche se entrambi sembrano apparire simili, esistono differenze tra di loro. Queste differenze possono riguardare la loro struttura, l'adesione, la forma geometrica, lo stato di ossidazione dell'azoto, la reattività chimica, gli usi di essi e simili.
L'ione è la base coniugata di HNO3 (acido nitrico V) che è un acido forte. È una molecola di planer con sp 3 ibridazione nell'atomo di azoto. Tutti e tre gli atomi di ossigeno sono equivalenti. Ci sono 24 elettroni nelle conchiglie di valenza. NO 3 - ione ha il peso molecolare di 62. 004 g mol -1 . NO 2 - ione è la base coniugata di HNO
2 (acido nitrico III) che è un acido debole (pKa = 3, 5). È anche una molecola planare con ibridazione sp 2 . Nella conchiglia di valenza, ci sono solo 18 elettroni. NO 2 - ion ha il peso molecolare di 46. 006 g mol -1 . Quando l'adesione in entrambi gli ioni sono considerati, in ioni NO 3 - il legame pi coinvolge quattro 2p
z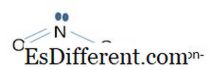

orbitali atomici (uno orbitla da N e tre orbitali da 3 atomi di ossigeno). Questi quattro orbitali atomici formano 4 orbitali molecolari pi a quattro centri. L'orbita molecolare con l'energia più bassa è l'orbitale di legame. L'orbitale con la più grande energia è l'orbita anti-legante. Altri due orbitali sono degenerati (uguali in energia) che sono orbitali non leganti. Nel caso di NO 2 - ion, il collegamento di pi coinvolge solo tre orbite atomiche 2p z . Qui l'orbitale con l'energia più bassa è l'orbitale di legame, il mezzo è l'orbitale non legante, l'altro è l'orbita antibondante. In entrambi gli ioni, le orbite di legame coinvolgono nel fare i legami σ (sigma-bond) ei non associati orbitali coinvolgono nel fare π-legami (pi-bonds). Pertanto, in NO 3 - ion ogni legame ha un ordine di legame di 1 1 / 3 . 1 da σ-bond e 1 / 3 dalle π-bond. In NO 2 - ion, l'ordine di legame è 1 1 / 2 . 1 da σ-bond e 1 / 2 dalle π-bond.
- ha una forma angolare (o V . Gli angoli di legame sono anche diversi. L'angolo di legame ONO di NO 3 - ione e NO 2 - ion sono 120 0 e 115 0 rispettivamente. Lo stato di ossidazione dell'azoto in entrambi i NO 3 - ione e NO 2 - ione sono rispettivamente +5 e +3.A causa di questi motivi (in particolare la differenza di legame), la reattività chimica (come la basicità, l'ossidazione / riduzione delle capacità, i prodotti di decomposizione termica dei composti sono costituiti da questi ioni) è anche diversa. In pratica, l'ione NO 2 - è una base più debole, mentre l'ione NO 3
- è una base molto più debole. Quando si prende in considerazione lo stato di ossidazione dell'atomo di azoto in questi ioni, il ione NO 2 - può agire come agente riducente così come un agente ossidante, mentre NO 3 - ione può agire solo come agente ossidante. Gli esempi per i prodotti ottenuti dalla decomposizione termica di NO 3 - e NO 2

- I composti contenenti ioni sono riportati di seguito per mostrare la differenza di reattività. Anche quando formano complessi con ioni metallici si comportano in modo dissimile. Il NO 2 - ione agisce come un legante monodentato mentre il NO 3

- ione agisce come un legante bidentato. Queste differenze nella reattività chimica ci aiutano a differenziare gli usi di essi. Ad esempio, i nitriti vengono generalmente utilizzati nella lavorazione della carne (a volte anche i nitrati vengono utilizzati) e nitrati vengono utilizzati per la produzione di esplosivi. I nitrati sono naturalmente presenti e sono cancerosi. Ma i nitriti non sono cancerosi.


