Differenza tra acetaldehide e acetone | Acetaldehyde vs Acetone
Differenza chiave - Acetaldehyde vs Acetone
Both Acetaldehyde e Acetone sono piccole molecole organiche, ma c'è una differenza tra loro basata sui loro gruppi funzionali. In altre parole, essi sono due diversi composti carbonilici con diverse proprietà chimiche e fisiche. L'acetone è il membro più piccolo del gruppo chetonico, mentre l'acetaldeide è il più piccolo membro del gruppo aldeidico. La differenza tra Acetaldehide e Acetone è il numero di atomi di carbonio nella struttura; acetone ha tre atomi di carbonio , ma acetaldehyde ha solo due atomi di carbonio. La differenza nel numero di atomi di carbonio e con due diversi gruppi funzionali portano a molte altre differenze nelle loro proprietà.
Che cosa è Acetone?
L'acetone è il più piccolo membro del gruppo ketone, noto anche come propanone . È un liquido incolore, volatile e infiammabile che viene utilizzato come solvente. La maggior parte dei solventi organici non si dissolve in acqua, ma l'acetone è miscibile con acqua. È molto usato per scopi di pulizia in laboratorio e come principale ingrediente attivo nei liquidi di rimozione dello smalto per unghie e in una vernice più sottile.

Che cosa è Acetaldehyde?
L'acetaldehyde, noto anche come ethanal è il membro più piccolo del gruppo aldeidico. È un liquido incolore e infiammabile con un forte odore soffocante. Ci sono molti usi industriali come la produzione di acido acetico, profumi, droghe e alcuni sapori.
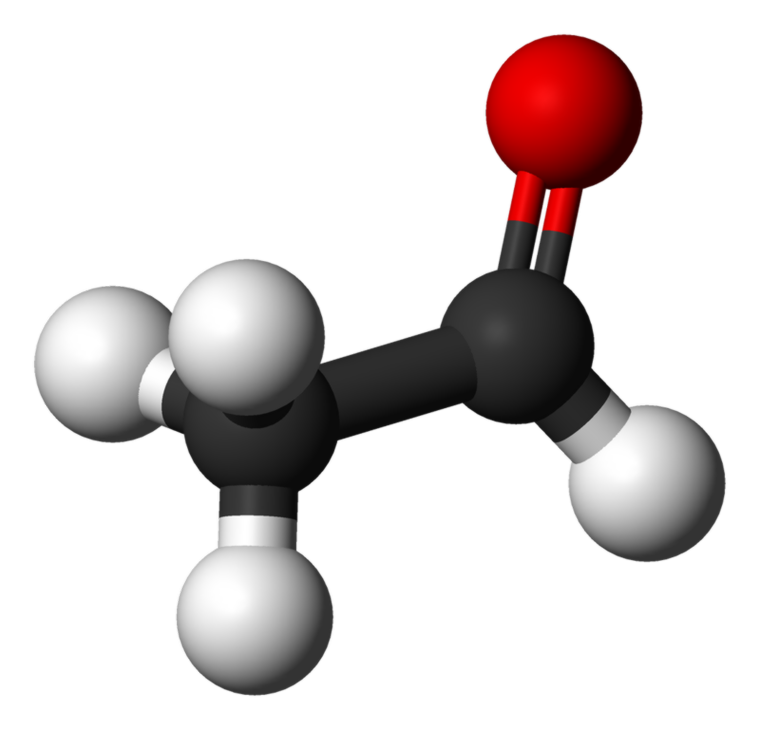
Qual è la differenza tra Acetaldehyde e Acetone?
Struttura e Proprietà Generiche di Acetaldehide e Acetone
Acetone: La formula molecolare dell'acetone C 3 H 6 O. È il membro più semplice della famiglia di chetoni. È un liquido volatile e infiammabile con odore pungente.

Acetaldehyde: La formula molecolare di acetaldeide C 2 H 4 O. È il più semplice e uno dei membri più importanti della famiglia di aldeidi. È un liquido incolore, volatile e infiammabile a temperatura ambiente.

Apparenza di Acetaldeide e Acetone
Acetone: In generale, l'acetone è presente nel sangue umano e nelle urine. Viene anche generato e smaltito nel corpo umano durante il normale metabolismo. Quando la gente ha diabetici, viene prodotta in quantità maggiori nel corpo umano.
Acetaldehyde: Acetaldehyde è naturalmente trovato in varie piante (caffè), pane, verdura e frutta matura.Inoltre, si trova nel fumo di sigaretta, gasolio e scarico diesel. Inoltre, è un intermediario nel metabolismo dell'alcool.
Usi di Acetaldeide e Acetone
Acetone: L'acetone viene utilizzato principalmente come solvente organico nei laboratori chimici ed è anche l'agente attivo nella produzione di un detergente per unghie e diluente nell'industria della vernice.
Acetaldehyde: Acetone è usato per produrre acido acetico, profumi, coloranti, agenti aromatizzanti e farmaci.
Caratteristiche dell'acetaldeide e dell'acetone
Identificazione
Acetone: L'acetone fornisce un risultato positivo per il test di iodoforme. Pertanto, può essere facilmente differenziata dall'acetaldeide usando il test di iodoforme.
Acetaldehyde: Acetaldehyde dà uno specchio d'argento al "reagente di Tollen" mentre i chetoni non danno un risultato positivo per questo test. Perché, non può ossidare facilmente. Il test di acido cromico e il reagente di Fehling possono anche essere usati per identificare l'acetaldeide.
Reattività
La reattività dei gruppi carbonilici (aldeidi e chetoni) è dovuta principalmente al gruppo carbonilico (C = O).
Acetone: In generale, i gruppi alchilici sono gruppi donatori di elettroni. L'acetone ha due gruppi metilici e diminuisce la polarizzazione del gruppo carbonile. Quindi, rende il composto meno reattivo. Due gruppi di metile attaccati ai due lati del gruppo carbonilico hanno portato a ulteriori ostacoli stearici. Pertanto, l'acetone è meno reattivo dell'acetaldeide.
Acetaldehyde: Al contrario, l'acetaldeide ha solo un gruppo metilico e un atomo di idrogeno legato al gruppo carbonilico. Poiché il gruppo metilico dona elettroni, l'atomo di idrogeno ritira gli elettroni; ciò rende la molecola più polarizzata e rende la molecola più reattiva. Rispetto all'acetone, l'acetaldeide ha meno effetti stearici e altre molecole possono avvicinarsi facilmente. A causa di queste ragioni, l'acetaldeide è più reattivo dell'acetone.



