Differenza tra gli elementi blocchi S e P | S vs P Elementi di blocco
Key Difference - S vs elementi di blocco P
La differenza tra gli elementi di blocco s e p può essere spiegata meglio utilizzando la loro configurazione elettronica. Negli elementi del blocco s, l'ultimo elettrone si riempie al sottosuolo s e negli elementi a blocchi p, l'ultimo elettrone si riempie nel sottosuolo p. Quando formano ioni; mentre gli elementi di blocco p accettano gli elettroni al sottogruppo p o rimuovono gli elettroni dal sottogruppo p. Alcuni elementi del gruppo p formano ioni positivi che rimuovono gli elettroni dall'estremità p-sottile e alcuni elementi (gli elementi più elettronegativi) formano ioni negativi che accettano un elettrone da altri. Quando si considerano le proprietà chimiche, c'è una differenza significativa tra gli elementi blocchi s e p; questo è fondamentalmente dovuto alla configurazione dell'elettrone.
Quali sono gli elementi S-block?
Elementi a blocchi S sono gli elementi chimici del gruppo I e del gruppo II nella tabella periodica. Poiché il sottosuolo può ospitare solo due elettroni, questi elementi hanno solitamente uno (gruppo I) o due (gruppo II) elettroni nella shell più esterna. Gli elementi del gruppo I e II sono mostrati sopra nella tabella.
-| 2 | Li | |
| Be | 3 | Na |
| Mg | 4 | IA |
| K | Ca | 5 |
| Rb | Sr | 6 |
| Cs | Ba | 7 |
| P. | Ra |
IA
| Metalli alcalini | II A |
| Metalli alcalini di terra | Tutti gli elementi in s bloccano ioni positivi e sono molto reattivi. |
Il posizionamento degli elementi S-Block nella Tabella Periodica
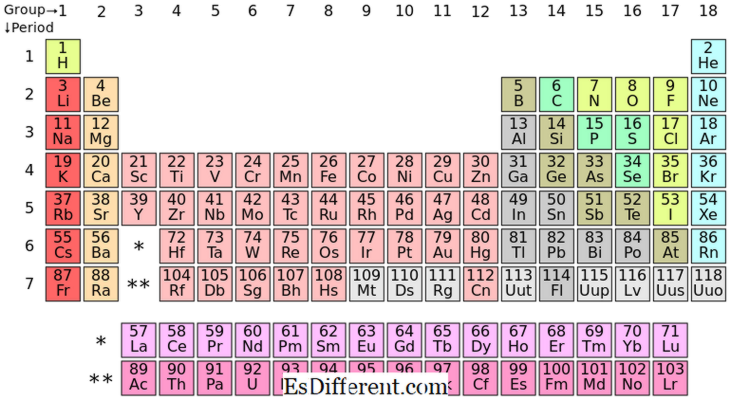
Gli elementi a blocco P sono gli elementi il cui ultimo elettrone riempie in sottosistema p. Ci sono tre p-orbitali; ogni orbitale può ospitare due elettroni, rendendo il totale di sei elettroni p. Pertanto, gli elementi di p-block hanno uno o sei elettroni p nella loro shell più esterna. Il blocco P contiene sia metalli che non metalli; inoltre ci sono alcuni metalloidi troppo.
13
| 14 | 15 | 16 | 17 | 18 | 2 | |
| B | C | N | O | F Ne | 3 | Al |
| Si | P | S | Cl | Ar | 4 | Ga |
| Ge | Come | Se | Br | Kr | 5 | in |
| Sn | Sb | Te | I | Xe | 6 | Tl |
| Pb Bi | Po | A | Rn | Qual è la differenza tra gli elementi blocchi S e P? | Elementi di blocco S: | Elementi a blocchi S hanno la configurazione comune di elettroni di [nobile gas] ns |
1
(per gli elementi del gruppo I) e [gas nobile] ns
2 (per gli elementi del gruppo II). Elementi a blocchi P: Gli elementi a blocchi P hanno la configurazione comune di elettroni di [nobile gas] ns 2 np
1-6 . Ma, l'elio ha 1s 2 configurazione; è una situazione speciale. Stati di ossidazione: Elementi S-block: Gli elementi a blocchi S non mostrano stati di ossidazione multipli come elementi a blocco p. Ad esempio, gli elementi del gruppo I mostrano uno stato di ossidazione +1 e gli elementi del gruppo II mostrano lo stato di ossidazione +2. Elementi a blocchi P:
A differenza degli elementi a blocchi a s, gli elementi di blocco p hanno uno stato di ossidazione comune per il rispettivo gruppo nella tabella periodica e altri altri stati di ossidazione aggiuntivi a seconda della stabilità dello ione.
Gruppo 13
14 15
| 16 | 17 | 18 | Configurazione elettronica generale | ns | 2 | np |
| 1 | ns 2 NP 2 | ns 2 NP 3 | ns 2 NP 4 ns | 2 ns 2 np | 6 1 st membro del gruppo | C N O |
| F E Numero di ossidazione comune | +3 | +4 | +5 | -2 | -1 | 0 |
| Altri stati di ossidazione | +1 | +2, -4 | +3, -3 | +4, +2, | +3, +5, 1, +7 | - |
| Proprietà: | Elementi S-block: | In generale, tutti gli elementi a blocchi s sono metalli. Sono lucidi, buoni conduttori elettrici e di calore e sono facili da rimuovere gli elettroni dalla shell di valenza. Sono gli elementi più reattivi della tabella periodica. | Elementi P-Block: | La maggior parte degli elementi a p-block sono non metallici. Hanno bassi punti di ebollizione, scarsi conduttori e difficili da rimuovere gli elettroni dalla shell più esterna. Invece, ottengono elettroni. Alcuni dei non metalli sono solidi (C, P, S, Se) a temperatura ambiente mentre alcuni sono gas (ossigeno, azoto). Il bromo è un non metallico ed è un liquido a temperatura ambiente. | Inoltre, p-block contiene alcuni elementi metallici; alluminio (Al), gallio (Ga), indio (In), stagno (Sn), talio (Tl), piombo (Pb) e bismuto (Bi). | Immagine gentile: |
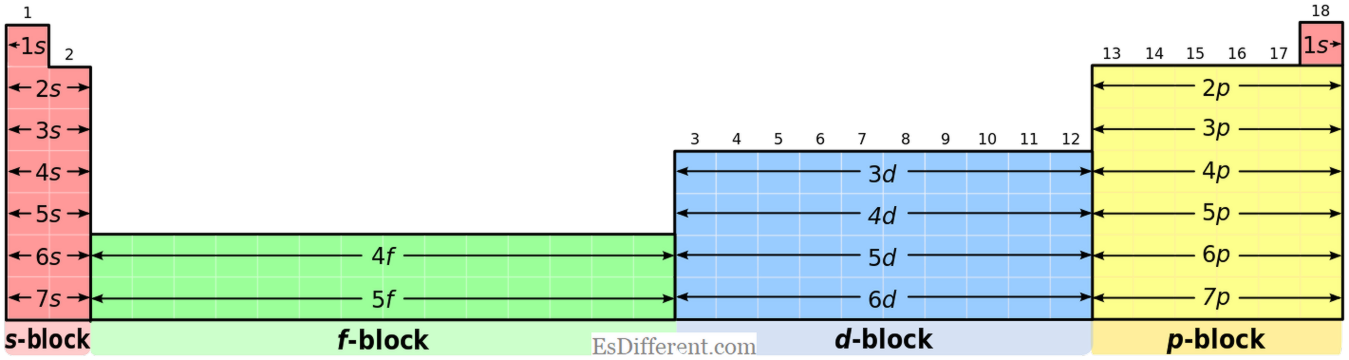
1. "Tavola periodica (poliatomica)" di DePiep [CC BY-SA 3. 0] via Commons
2. "Blocchi periodici della tabella spdf (32 colonne)" da Utente: DePiep [CC BY-SA 3. 0] via Commons




